概要
分子イメージングとは、生体内で行われている細胞レベル・分子レベルの活動を画像化することです。当分子イメージング研究部は、生体機能を画像化する「PET」という診断技術を活用し、疾患の病態解明や新薬開発に取り組んでいます。
当研究部の主なミッションとして、PETに関する治験薬製造と治験実施、臨床研究、撮像・解析法開発と品質管理があります。また市民病院として、臨床研究を通じて得られた最先端の研究成果を市民の皆様に提供する体制づくりに努めております。これまでに培った創薬・撮像・品質管理のノウハウを最大限に活用し、PETを用いた安全かつ有効性の高い診断技術を開発し、医療の進歩に貢献していきます。
PET治験薬製造事業
日本有数のPET治験薬GMP体制を完備
当研究部は、2008年にPET治験を開始し、2011年には治験薬GMP基準に適合したホットラボを新たに整備しました*1。これらの実績とインフラが高く評価され、国内外の製薬企業からさまざまなPET治験薬製造を受託しています。当院で製造されたPET治験薬は、当院で実施される治験に加え、近隣の医療機関にも輸送され使用されています。
当院は、小型サイクロトロンと2つのPET薬剤製造ホットラボエリア(治験薬GMP対応ラボと学会GMP対応ラボ)を保有しています。PET薬剤を治験に使用する場合は、世界基準のクリーン度と高度な品質管理、品質保証が要求されるため、治験薬GMP対応ラボを使用しています。
PET治験薬の製造はパートナー事業者と連携し、PET薬剤の製造や管理の専門家が対応します。これまでの経験を活かし、単なる薬剤製造のみならず、国内外の法規制への対応や関係書類の整備についても、依頼企業などにアドバイスしています。さらに、近年世界中で注目を集めるtheranostics(セラノスティクス:診断と治療の融合)に対応すべく、アルファ線やベータ線核種を標識した核医学治療製剤についても、治験薬製造拠点としての整備を進めていきます。
治験以外にも、臨床研究用のためのPET薬剤製造も多数実施しており、新しいPET薬剤の合成方法の開発や改良の研究も行われています。
*1当時は「先端医療センター」として実施しました。先端医療センターは2017年11月に神戸市立医療センター中央市民病院に移管統合されました。
- Iimori H, Hashizume Y, Sasaki M, et al. First automatic radiosynthesis of 11C labeled Telmisartan using a multipurpose synthesizer for clinical research use. Ann Nucl Med. 2011;25:333-337.
PET治験
経験豊富なスタッフがあらゆるタイプのPET治験に対応
PET治験では、時々刻々と放射能が減衰する放射性薬剤を取り扱います。それ以外にも、被験者の取扱い、撮像、画像処理など、他の一般的な医薬品の治験と異なる要素があります。当院ではPET治験に関して経験豊かなスタッフ(医師、診療放射線技師、看護師、治験コーディネーター)が、万全の体制で対応します。
当院はPET/CT装置3台を保有しています。うち1台は治験・臨床研究専用として使用しており、治験スケジュールに合わせた柔軟な対応が可能です。治験薬製造施設と撮像施設が一体化していることから、あらゆるPET薬剤の条件に合わせた対応が可能です。18F標識製剤以外にも、11Cや68Gaなど、ほかの核種を用いたPET治験にも対応できます。
PET治験の種類
PET治験には、薬物動態試験、治療薬治験でのサロゲートマーカーとしてのPET治験、PET診断薬としての治験など、いくつかのタイプがあります。
薬物動態試験
治療薬のヒトにおける臓器の体内動態を把握することができれば、標的臓器への分布を見ることで薬効を予測することができます。また、また標的組織以外への分布を見ることで副作用を予測することも可能です。候補化合物をポジトロン放出核種で標識することができる場合は、PETによる薬物動態試験が可能となります。治療薬が薬理作用を発現する濃度よりずっと低い物質量(マイクロドーズ)の投与で、その全身分布を把握する場合はPETマイクロドーズ試験(Phase-0)となり、通常のPhase-I試験よりも容易に実施できます。このような手法にPETを活用することで、治験をより効率的に実施できることが期待されます。
サロゲートマーカーとしてのPET治験
治験は薬効に応じたゴール(エンドポイント)の設定が必要で、通常は症状消失、検査値の改善、無再発生存や総生存の延長などが設定されます。しかしなかには、その評価が容易でない場合もあります。疾患の原因となる臓器や体内組織が明らかで病態の本質(代謝や受容体などの生物学的性質)を評価できるPET薬剤があれば、PETを代替的な治療指標(サロゲートマーカー)として活用できます。また、治験の被験者をリクルートする際にも、PETをマーカーとして利用できます。
とくに治療薬の標的(ターゲット)を評価できるPET薬剤があればきわめて有用です。たとえばアルツハイマー病治療薬の治験においては脳内アミロイドやタウの沈着が、精神疾患の治療薬の治験では脳の受容体やトランスポータがPETで評価されています。抗悪性腫瘍薬の治験では、糖代謝、受容体、血管新生、免疫反応などがそれぞれPETで評価可能です。このような治療薬治験でのPETによる被験者選択と薬理効果の評価は、他によい評価方法が無い疾患や治療薬で重宝され、とくに早期相治験での用量設定や以後の開発方針決定に役立ちます。なお、ここで用いられるPET薬剤は診断薬として承認されている必要はなく、承認申請を前提とする必要もありません。
診断薬としてのPET医薬品の治験
画像診断的手法として一般に使用されるCTやMRIはおもに形態を評価するものですが、PETは機能を評価することができます。この特徴を活かし、疾患の鑑別や機能評価を従来よりも正確に行い、患者を治療方針によって層別化できることがPETに期待されます。PET診断薬は半減期が短いため、わが国では医薬品として承認されるほか、院内製造のための合成装置が医療機器として承認されています。現在わが国で承認されているPET診断薬は、悪性腫瘍を主な対象疾患とする18F-FDGなど数種類に限られています。一方で、脳、心臓、腫瘍、炎症等を対象とした多くのPET診断薬が国内外で研究開発されており、そのために診断薬としての有効性を評価する治験が行われます。さらに基礎研究分野においても多くの候補薬があり、今後多くのPET診断薬の登場が待たれます。なおPET診断薬の第I相治験では、安全性確認と標的臓器への集積以外に、経時採血による血中薬物動態と血中標識代謝物の測定や、全身撮像の繰り返しによる被ばく線量の測定といった、通常のPET撮像とは全く異なる測定が行われます。
このようにPETを有効活用することで、治験をよりスムーズに進められることが期待されています。
当院の分子イメージング研究部では、アミロイドPET薬剤やタウPET薬剤の第I相治験を実施したほか、アルツハイマー病治療薬治験でのこれらのPET薬剤によるPET試験をさかんに行っています。被験者の募集についても、KOBEもの忘れネットワークといった仕組みを活用し、すみやかな治験が実施できるよう協力しています。
- Ohnishi A, Akamatsu G, Ikari Y, et al. Dosimetry and efficacy of a tau PET tracer [18F]MK-6240 in Japanese healthy elderly and patients with Alzheimer’s disease. 2023;37:108-120.
- Nakano M, Nakamura T, Takita Y, et al. Radiation dosimetry and pharmacokinetics of florbetapir (18F) in Japanese subjects. Ann Nucl Med. 2019;33:639-645.
- Miki T, Shimada H, Kim JS, et al. Brain uptake and safety of Flutemetamol F 18 injection in Japanese subjects with probable Alzheimer’s disease, subjects with amnestic mild cognitive impairment and healthy volunteers. Ann Nucl Med. 2017;31:260-272.
- Senda M, Yamamoto Y, Sasaki M, et al. An exploratory efficacy study of the amyloid imaging agent [18F]flutemetamol in Japanese Subjects. Ann Nucl Med. 2015;29:391-399.
- Senda M, Brooks DJ, Farrar G, et al. The clinical safety, biodistribution and internal radiation dosimetry of flutemetamol (18F) injection in healthy Japanese adult volunteers. Ann Nucl Med.
- Senda M, Sasaki M, Yamane T, et al. Ethnic comparison of pharmacokinetics of 18F-florbetaben, a PET tracer for beta-amyloid imaging, in healthy Caucasian and Japanese subjects. Eur J Nucl Med Mol Imaging. 2015;42:89-96.
PET臨床研究
他施設からの研究PETも受託
治験以外に、PETを利用した臨床研究にも積極的に取り組んでいます。未承認PET薬剤を院内製造し、疾患の病態生理の解明、対象患者の層別化、PET薬剤の有効性に関する臨床研究を行っております。対象は、さまざまな悪性腫瘍、アルツハイマー病、パーキンソン病など多岐にわたります。ヒトを対象とするPET薬物動態試験や、世界初となるPET薬剤をヒトに初めて投与するFirst-in-human試験を実施し、安全性、有効性、全身分布等を評価しました。また、アルツハイマー病をテーマとする国家プロジェクトであるJ-ADNIやAMEDプレクリニカルプロジェクトなどに参加しました。
他の医療機関からの研究PET撮像依頼や、共同研究も受けています。PETを用いた臨床研究を行いたいが自施設にPETが無い、あるいはPETがあっても臨床研究に対応していない、という場合など、お気軽にご相談ください。
現在実施中の臨床研究(介入研究)
分子イメージング研究部では、院内診療科、院外医療機関と連携し、PETを用いた以下の介入研究を実施しています。
| 研究課題名・概要 | 参照 |
| 【優性遺伝アルツハイマーネットワーク (DIAN-J) 】 米国のワシントン大学(セントルイス)が主導する遺伝性のアルツハイマー病に対する世界的な研究です。本研究では、18F-FDG・11C-PiBのPET検査を実施します。 |
研究ウェブサイト |
| 【J-TRCオンサイト研究】 全国規模で実施される認知症の研究で、治験に参加できる方を集めることを目的としたものです。本研究では、18F-florbetapir PET検査を実施します |
UMINリンク |
| 【側頭極研究】 左側頭極の変性を伴う進行性失語症の病態について調べる研究です。本研究では、18F-florbetapir・18F-FDG・18F-MK6240のPET検査を実施します。 |
UMINリンク |
| 【PAD-TRACK研究】 プレクリニカル期のアルツハイマー病がどのように進行していくのかを調べる全国規模の多施設研究です。本研究では、18F-florbetapir・18F-MK6240のPET検査を実施します。 |
jRCTリンク |
| 【高齢高度難聴者の脳代謝に対する人工内耳装用の影響】 当院の総合聴覚センター主導で実施される研究です。本研究では、18F-FDG PET検査を実施します。 |
総合聴覚センターリンク |
| 【酸素ガスPET研究】 Discovery IQというPET/CT装置での酸素-15ガスPET検査法を確立するための研究です。本研究では、15O-O2・15O-CO2・15O-COのPET検査を実施します。 |
UMINリンク |
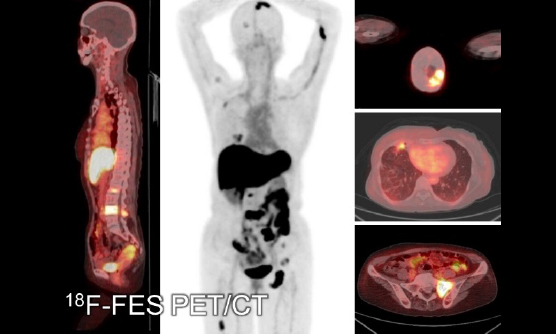
| 【乳癌のFES-PET研究】 乳癌におけるエストロゲン受容体PETと血液中の遊離DNAとの関係性を調べる研究です。本研究では、18F-FES PET検査を実施します。 |
UMINリンク |
| 【腫瘍FAPI-PET研究】 FAPIという新しいPET薬剤が、悪性腫瘍の方(疑い含む)でどのように描出されるのかを調べる研究です。本研究では、18F-FAPI-74のPET検査を実施します。 |
UMINリンク |
| 【腎臓FAPI-PET研究】 FAPIという新しいPET薬剤が腎臓に集まる様子を評価して、腎臓の線維化に関する指標と関連するかを調べる研究です。本研究では、18F-FAPI-74のPET検査を実施します。 |
UMINリンク |
|
【肝臓がんFAPI-PET研究】 |
UMINリンク |
|
【18F-AF78のfirst-in human PET研究】
|
jCRTリンク |
既存の資料を用いた観察研究
当研究部では、既存の診療情報(カルテに記載されている日常診療で得られた情報)や過去に実施された研究データを利用し、PET検査と診療情報(経過や検査結果など)との関係性を検証する研究も行っています。こういった研究を、観察研究と言います。観察研究についても、当院の倫理委員会で審査を受け、承認を受けた上で実施されます。データは匿名化された上で解析され、個人情報が外部に漏れることは一切ありません。
観察研究は、対象となる方に対して侵襲的なことを実施したり、治療に影響を与えたりするものでないことから、都度同意を得る必要は無いことが国の指針により認められています。しかし一方で、研究の目的を含め、研究の実施についての情報を通知または公開し、さらに可能な限り拒否できる機会を保証することが必要とされています。
以下に当研究部で実施する観察研究の内容を掲示します。研究の対象に含まれている方で、ご自分のデータを利用してほしくない場合は、お手数ですが以下の問い合わせ先までご連絡下さい。研究の趣旨についてご理解いただき、医学の発展のためご協力を賜りますようお願い申し上げます。
| 現在実施中の、既存の資料を用いた観察研究はありません | ー |
| 研究課題名・概要 | 参照 |
問い合わせ先
神戸市立医療センター中央市民病院 分子イメージング研究部 部長 山根 登茂彦
神戸市中央区港島南町2丁目1−1
TEL 078-302-4321(代)
- Ohnishi A, Yamane T, Shimizu K, et al. False‑positive [18F]FAPI‑74 uptake caused by blood retention due to external jugular vein thrombus: Pitfall in the early‑phase scan. Eur J Nucl Med Mol Imaging. 2024.
- Senda M, Ishii K, Ito K, et al. A Japanese multicenter study on PET and other biomarkers for subjects with potential preclinical and prodromal Alzheimer’s disease. J Prev Alzheimers Dis. 2021;8;495-502.
- Watanabe Y, Mawatari A, Aita K, et al. PET imaging of 11C-labeled thiamine tetrahydrofurfuryl disulfide, vitamin B1 derivative: First-in-human study. Biochem Biophys Res Commun. 2021;555:7-12.
- Akamatsu G, Ohnishi A, Aita K, et al. A revisit to quantitative PET with 18F-FDOPA of high specific activity using a high-resolution condition in view of application to regenerative therapy. Ann Nucl Med. 2017;31:163-171.
- Ohnishi A, Senda M, Yamane T, et al. Exploratory human PET study of the effectiveness of 11C-ketoprofen methyl ester, a potential biomarker of neuroinflammatory processes in Alzheimer’s disease. Nucl Med Biol. 2016;43:438-444.
- Ohnishi A, Senda M, Yamane T, et al. Human whole-body biodistribution and dosimetry of a new PET tracer, [11C]ketoprofen methyl ester, for imagings of neuroinflammation. Nucl Med Biol. 2014;41:594-599.
- Yamane T, Takaoka A, Kita M, Imai Y, Senda M. 18F-FLT PET performs better than 18F-FDG PET in differentiating malignant uterine corpus tumors from benign leiomyoma. Ann Nucl Med. 2012;26:478-484.
- Maeda K, Ohnishi A, Sasaki M, et al. Quantitative investigation of hepatobiliary transport of [11C]telmisartan in humans by PET imaging. Drug Metab Pharmacokinet. 2019;34:293-299.
- Shimizu K, Takashima T, Yamane T, et al. Whole-body distribution and radiation dosimetry of [11C]telmisartan as a biomarker for hepatic organic anion transporting polypeptide (OATP) 1B3. Nucl Med Biol. 2012;39:847-853.
- Kikuchi M, Yamane T, Shinohara S, et al. 18F-fluoromisonidazole positron emission tomography before treatment is a predictor of radiotherapy outcome and survival prognosis in patients with head and neck squamous cell carcinoma. Ann Nucl Med. 2011;25:625-633.
- Yamane T, Kikuchi M, Shinohara S, Senda M. Reduction of [18F]fluoromisonidazole uptake after neoadjuvant chemotherapy for head and neck squamous cell carcinoma. Mol Imaging Biol. 2011;13:227-231.
- Yamane T, Sakamoto S, Senda M. Clinical impact of 11C-methionine PET on expected management of patients with brain neoplasm. Eur J Nucl Med Mol Imaging. 2010;37:685-690.
- Senda M, Kubo N, Adachi K, et al. Cerebral histamine H1 receptor binding potential measured with PET under a test dose of olopatadine, an antihistamine, is reduced after repeated administration of olopatadine. J Nucl Med. 2009;50:887-892.
PET精度管理
PET精度管理・多施設研究コア
より精度の高いPET撮像・健全なPET研究を推進
PETはその性質上、画質と定量値や診断能が、用いる撮像装置(PETカメラ)や撮像方法の詳細と画像の評価解析方法に依存します。したがって、信頼性の高い普遍的な検査法として確立させるには、方法の標準化が必要です。また、撮像方法や画像解析方法を工夫することによって、新たな情報や精度の高い情報が得られることもあります。当研究部では、このような方法論の研究開発にも取り組んでいます。
脳の多施設臨床研究のPETコアと標準化
多施設PET臨床研究では、必然的にPET施設によってPETカメラが異なります。施設によって経験や体制もさまざまです。信頼性のある多施設PETデータベースを構築し、PETのイメージングバイオマーカーとしての健全な利用を推進するには、標準化とデータの品質管理が必要です。アルツハイマー病をテーマとする多施設臨床研究の国家プロジェクトであるJ-ADNIやAMEDプレクリニカルプロジェクトでは、当院にてPET撮像を行うことに加え、多施設研究の「PETコア」として全国の参加PET施設のPET撮像の標準化とデータの品質管理を行うという大きな役割を担いました。脳のFDGやアミロイドPETに対するPETコアとしての成果は、その後日本核医学会による標準的プロトコールとPET撮像施設認証制度に採用されて当該プロジェクト以外にも普及し、全国のPET施設における質の向上に役立っています。
- Ikari Y, Akamatsu G, Matsumoto K, Yamane T, Senda M, Fukuchi K, AMED Preclinical AD Study Investigators. Improved correlation of 18F-Flortaucipir PET SUVRs and clinical stages in the Alzheimer disease continuum with the MUBADA/PERSI-based analysis. J Nucl Med Technol. 2024.
- Senda M. Standardization of PET imaging and site qualification program by JSNM: collaboration with EANM/EARL. Ann Nucl Med. 2020;34:873-874.
- Akamatsu G, Ikari Y, Ohnishi A, et al. Voxel-based statistical analysis and quantification of amyloid PET in the Japanese Alzheimer’s disease neuroimaging initiative (J-ADNI) multi-center study. EJNMMI Res. 2019;9:91.
- Akamatsu G, Nishio T, Adachi K, Ikari Y, Senda M. Whole-body biodistribution and the influence of body activity on brain kinetic analysis of the 11C-PiB PET scan. Radiol Phys Technol. 2017;10:464-474.
- Yamane T, Ishii K, Sakata M, et al. Inter-rater variability of visual interpretation and comparison with quantitative evaluation of 11C-PiB PET amyloid images of the Japanese Alzheimer’s Disease Neuroimaging Initiative (J-ADNI) multicenter study. Eur J Nucl Med Mol Imaging. 2017;44:850-857.
- Akamatsu G, Ikari Y, Nishio T, et al. Optimization of image reconstruction conditions with phantoms for brain FDG and amyloid PET imaging. Ann Nucl Med. 2016;30:18-28.
- Ikari Y, Akamatsu G, Nishio T, et al. Phantom criteria for qualification of brain FDG and amyloid PET across different cameras. EJNMMI Phys. 2016;3:23.
- Yamane T, Ikari Y, Nishio T, Ishii K, Ishii K, Kato T, et al. Visual-statistical interpretation of 18F-FDG-PET images for characteristic Alzheimer patterns in a multicenter study: inter-rater concordance and relationship to automated quantitative evaluation. AJNR Am J Neuroradiol. 2014;35:244-9.
- Ikari Y, Nishio T, Makishi Y, et al. Head motion evaluation and correction for PET scans with 18F-FDG in the Japanese Alzheimer’s disease neuroimaging initiative (J-ADNI) multi-center study. Ann Nucl Med. 2012;26:535-544.